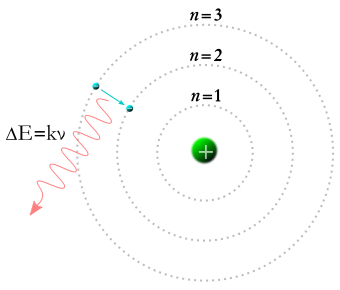
* هذه الصورة توضخ نموذج ذرة الإيدروجين الذي إقترحه بوهر. الإلكترون يدور في مدار حول النواة
و يمكن أن يغير مداره من الداخل إلى أعلى عندما يكتسب طاقة من الخارج . ويطرد هذه الطاقة المكتسبة على هيئة فوتون ((كمومي)) ، أي على هيئة شعاع ذو تردد محدد وبالتالى طاقة محددة ، عندما يقفز الإلكترون من مستوى طاقة المدار العلوي إلى مستوي طاقة مدار سفلى ، كما في الشكل.
هذا هو طيف غاز الإيدروجين المثار عند درجة حرارة عالية كما حصل عليه العالم الدنمركي لايمن أواخر القرن التاسع عشر . ولاحظ أن خطوط الطيف منفصلة عن بعضها ، وكل خط منها (أي شعاع ضوء فوتون) يتميز بطول موجة محددة .
بالنسبة للذرات التي تكون في شكل بلـّورات صلبة ، يمكن تحديد المسافة بين نواتين متجاورتين وبالتالى يمكن عمل حساب تقديري لحجم الذرة . والذرات التي لا تشكل بلـّورات صلبة يتم استخدام تقنيات أخرى تتضمن حسابات تقديرية . فمثلا حجم ذرة الهيدروجين تم حسابها تقريبيا على أنه 1.2× 10−10 م . بالمقارنة بحجم البروتون وهو الجسيم الوحيد في نواة ذرة الهيدروجين 0.87× 10−15 م . وعلى هذا فإن النسبة بين حجم ذرة الهيدروجين وحجم نواتها تقريبا 100,000 .وتتغير أحجام ذرات العناصر المختلفة ، ويرجع ذلك لأن العناصر التي لها شحنات موجبة أكبر في نواتها تقوم بجذب إلكترونات بقوة أكبر ناحية النواة .
.....
التوقيع متل قلتو..
ان كتبنا او لأ ما بيتغير شي !!
**
ف أنو ,,ما عندي شي قولو..!
***
D: